Плазменные факторы свертывания. Факторы свёртывания крови ♥
|
Функция активной формы |
||
|
Фибриноген |
Образует фибриновый гель |
|
|
Протромбин |
Активирует фибриноген (сериновая протеаза) |
|
|
Тканевой тромбопластин |
Стимулирует активацию ф VII(внешний путь; белок-субстрат) На данный момент он появляется в просвете сосудов в результате его стимуляции цитокинами: интерлейкин 1 и фактор некроза опухоли. Этот белково-фосфолипидный комплекс хорошо представлен мозгом, плацентой, яичкой, бляшкой, моноцитами и сосудистым эндотелием. Коагуляционные кофакторы имеют пространственно-активные протеазы в идеальном положении на поверхности тромбоцитов крови, чтобы обеспечить их взаимодействие в оптимальных условиях. Этот фактор представляет собой гликопротеин, активация которого является общей целью внутренних и внешних путей коагуляции. |
|
|
Ионы кальция |
Необходимы для взаимодействия факторов свертывания с фосфолипидной поверхностью |
|
|
Проалекрин |
Стимулирует активацию ф II (белок-субстрат) |
|
|
Проконвертин |
Активирует ф Х (сериновая протеаза) |
|
|
Антигемофильный фактор А Важную роль в этом процессе играют тромбоциты. Последний является альфа2 неферментативным глобулином плазмы, который действует как кофактор в процессе коагуляции. Этот фактор, главным образом синтезированный в печени, состоит из двух пар пептидных цепей, присутствует в плазме как инертный идиоген и активируется в результате действия тромбина, ионов кальция и Ха. Включение антиплазмина альфа2 в фибриновую сеть приводит к повышенной резистентности к плазмину. Этот фактор, по-видимому, стимулирует ответ фибрин-фибронектин-коллаген и пролиферацию фибробластов, благоприятствуя образованию рубцов. В зависимости от их роли в гемостазе, факторы коагуляции плазмы можно разделить на. |
Стимулирует активацию ф Х (белок-субстрат) |
|
|
Антигемофильный фактор В |
Стимулирует ф Х (сериновая протеаза) |
|
|
Фактор Стюарта-Прауэра |
Активирует ф II (сериновая протеаза) |
|
|
Предшественник плазменного тромбопластина Первичный и вторичный гемостаз. Активация коагуляционных факторов. Основными принципами коагуляционного каскада являются. Триггеры и разворачивают ферментативные реакции в каскаде факторов коагуляции плазмы. Эти процессы включают последовательную активацию плазменных зимогенов с помощью сериновых протеаз. Каждая протеаза катализирует в этом случае следующую реакцию зимоген-протеазы путем расщепления пептидных связей. Результатом этого плазмообразующего каскада является образование тромбина. Трансформация растворимого фибриногена в нерастворимый фибрин под действием тромбина. Каждая реакция, которая возникает во время каскада, является результатом сборки комплекса, состоящего из фермента, субстрата и кофактора. Эти компоненты обычно собирают на фосфолипидный комплекс и связывают через ионы Са. |
Активирует ф IX (сериновая протеаза) |
|
|
Фактор Хагемана |
Активирует ф XI (сериновая протеаза) |
|
|
Фибринстабилизирую-щий фактор |
Стабилизирует фибриновую сеть (трансглутаминаза) |
|
|
Прекалликреин (фактор Флетчера) Они действуют путем выравнивания активирующего белка и гипогена субстрата с фосфолипидной поверхностью тромбоцитов в идеальных положениях для их взаимодействия. После активации каскад коагуляции должен быть ограничен повреждениями сосудов, чтобы предотвратить коагуляцию по циркулирующему дереву. Процесс коагуляции включает в себя ряд прокоагулянтных факторов, которые имеют тройное происхождение: плазма, ткани и тромбоциты крови. Этапы коагуляции состоят из. Генерация протромбиназы. Формирование и стабилизация фибрина. Тромбодинамическая фаза коагуляции. Упрощенная схема внешних путей коагуляции. Клетки периваскулярного поражения ткани высвобождают клеточный флюид, который содержит тромбопластин ткани и фосфолипид-цефалин. |
Активация плазминогена |
|
|
Кининоген высокомолелекулярный (фактор Фитцджеральда – Фложе) |
Фактор контактной активации |
|
|
Протеин С |
Инактивация активированных факторов Vи XIII |
|
|
Протеин S |
Стимулирует инактивацию факторов активированным протеином С Он адсорбируется на коллагеновых волокнах поражения и активирует его превращение в кинин. Протромбиназа, когда-то образовавшаяся, будет протромбином при тромбине. Диаграмма коагуляции. По собственному действию: протромбиназа, образующаяся таким образом в больших количествах, действует на протромбин, поглощая его в тромбин и 2 белковые фракции. Тромбин также имеет другие роли в процессе гемостаза: он непосредственно индуцирует агрегацию и секрецию тромбоцитов, активирует сосудистый эндотелий, создавая молекулы адгезии лейкоцитов и различные другие медиаторы. Кроме того, воспалительные фокальные моноциты могут быть активированы непосредственно действием тромбина. |
|
|
Фактор Виллебранда |
Опосредует связывание тромбоцитов с субэндотелием |
Большинство плазменных факторов свертывания крови образуется в печени. Для синтеза некоторых из них (II, VII, IX, X) необходим витамин К, содержащийся в растительной пище и синтезируемый микрофлорой кишечника. При недостатке или снижении активности факторов свертывания крови может наблюдаться патологическая кровоточивость. Это может происходить при тяжелых и дегенеративных заболеваниях печени, при недостаточности витамина К. Витамин К является жирорастворимым витамином, поэтому его дефицит может обнаружиться при угнетении всасывания жиров в кишечнике, например при снижении желчеобразования. Эндогенный дефицит витамина К наблюдается также при подавлении кишечной микрофлоры антибиотиками. Ряд заболеваний, при которых имеется дефицит плазменных факторов, носит наследственный характер. Примером являются различные формы гемофилии, которыми болеют только мужчины, но передают их женщины.
Это подразумевает два процесса: - трансформация фибриногена на фибрине. Этот процесс происходит при наличии тромбоцитарного фактора 2, высвобождаемого из тромбоцитов крови во время сосудистой метаморфозы. После образования мономеров фибрина они подвергаются двум процессам полимеризации. После двойной полимеризации рождается растворимый лабильный фибриновый сгусток. На этом этапе явление обратимо.
В сетках сформированной сетки фибрина захватываются эритроциты, образуя так называемый красный сгусток. Одновременно с процессом образования фибрина рефлекторная вазоконстрикция производится в сосудистое время гемостаза химическими веществами, такими как серотонин, высвобождаемый тромбоцитами крови во время явления высвобождения.
Вещества, находящиеся в тромбоцитах, получили название тромбоцитарных, или пластинчатых, факторов свертывания крови. Их обозначают арабскими цифрами. К наиболее важным тромбоцитарным факторам относятся: ПФ-3 (тромбоцитарный тромбопластин) – липидно-белковый комплекс, на котором как на матрице происходит гемокоагуляция, ПФ-4 – антигепариновый фактор, ПФ-5 – благодаря которому тромбоциты способны к адгезии и агрегации, ПФ-6 (тромбостенин) – актиномиозиновый комплекс, обеспечивающий ретракцию тромба, ПФ-10 – серотонин, ПФ-11 – фактор агрегации, представляющий комплекс АТФ и тромбоксана.
После его образования стабилизированный фибриновый сгусток фиксирует фибробласты из перилезии соединительной ткани. Фибронектин считается адгезивным гликопротеином, который распознается специфическими клеточными рецепторами, называемыми интегринами. Основным источником плазменного фибронектина является гепатоцит, но он также продуцируется эндотелием сосудов, фибробластами и макрофагами.
Таким образом, ткань становится более однородно структурированной, увеличивая ее механическую прочность. Таким образом образуется гомогенная слабая гомологичная сшивка с уменьшенным объемом 15% по сравнению с ранее сформированным шприцем, в структуре которого имеются тромбоциты крови, ответственные за следующий процесс восстановления.
Аналогичные вещества открыты и в эритроцитах, и в лейкоцитах. При переливании несовместимой крови, резус-конфликте матери и плода происходит массовое разрушение эритроцитов и выход этих факторов в плазму, что является причиной интенсивного внутрисосудистого свертывания крови, При многих воспалительных и инфекционных заболеваниях также возникает диссеминированное (распространенное) внутрисосудистое свертывание крови (ДВС-синдром), причиной которого являются лейкоцитарные факторы свертывания крови.
Корректировка процесса коагуляции. В отсутствие контрольных и самоограничивающих систем процесс коагуляции будет превышать допустимые физиологические пределы, он будет потреблять все количество доступного субстрата для каждого сосудистого микроузла с пагубным воздействием на организм.
Система ингибирования коагуляции состоит из физиологических ингибиторов коагуляции и патологических ингибиторов. Как правило, тест для определения концентрации фактора Х выполняется для выявления причин, вызывающих непрерывное кровотечение. Вы должны поговорить с врачом. Это первый и самый важный шаг в подготовке к тесту. Врач спросит вас, будете ли вы следовать определенным методам лечения и закажите их прекращение, если есть риск повлиять на результаты теста. Врач должен также объяснить связанные с этим риски, как будет проводиться тест и какие результаты будут указаны.
По современным представлениям в остановке кровотечения участвуют 2 механизма: сосудисто-тромбоцитарный и коагуляционный.
Сосудисто-тромбоцитарный гемостаз
Благодаря этому механизму происходит остановка кровотечения из мелких сосудов с низким артериальным давлением. При травме наблюдается рефлекторный спазм поврежденных кровеносных сосудов, который в дальнейшем поддерживается сосудосуживающими веществами (серотонин, норадреналин, адреналин), освобождающимися из тромбоцитов и поврежденных клеток тканей. Внутренняя стенка сосудов в месте повреждения изменяет свой заряд с отрицательного на положительный. Благодаря способности к адгезии под влиянием фактора Виллебранда, содержащегося в субэндотелии и кровяных пластинках, отрицательно заряженные тромбоциты прилипают к положительно заряженной раневой поверхности. Практически одновременно происходит агрегация – скучиванье и склеивание тромбоцитов с образованием тромбоцитарной пробки, или тромба. Сначала под влиянием АТФ, АДФ и адреналина тромбоцитов и эритроцитов образуется рыхлая тромбоцитарная пробка, через которую проходит плазма (обратимая агрегация). Затем тромбоциты теряют свою структурность и сливаются в однообразную массу, образуя пробку, непроницаемую для плазмы (необратимая агрегация). Эта реакция протекает под действием тромбина, образующегося в небольших количествах под действием тканевого тромбопластина. Тромбин разрушает мембрану тромбоцитов, что ведет к выходу из них серотонина, гистамина, ферментов, факторов свертывания крови. Пластинчатый фактор 3 дает начало образованию тромбоцитарной протромбиназы, что приводит к образованию на агрегатах тромбоцитов небольшого количества нитей фибрина, среди которых задерживаются эритроциты и лейкоциты. После образования тромбоцитарного тромба происходит его уплотнение и закрепление в поврежденном сосуде за счет ретракции кровяного сгустка. Ретракция осуществляется под влиянием тромбостенина тромбоцитов за счет сокращения актин-миозинового комплекса тромбоцитов. Тромбоцитарная пробка образуется в целом в течение 1 – 3 минут с момента повреждения, и кровотечение из мелких сосудов останавливается.
Вам нужно будет предоставить образец крови. Лицо, выполняющее эту операцию, должно выполнить следующие шаги. Вены будут увеличиваться, делая вставку иглы в вену гораздо более безопасным процессом. Область, в которую вставлена игла, должна быть очищена спиртом, и в вену будет введена игла. Кровь будет собираться в специальном контейнере. сбор был удален, игла была удалена, гараж был удален, а покрытая иглой область была покрыта марлей. Повяжите по мере необходимости.
- Чтобы остановить кровообращение, гараж будет обернут вокруг верхней части руки.
- Держите давление на ударах, чтобы остановить кровотечение.
В крупных сосудах тромбоцитарный тромб не выдерживает высокого давления и вымывается. Поэтому в крупных сосудах гемостаз может быть осуществлен путем формирования более прочного фибринового тромба, для образования которого необходим ферментативный коагуляционный
механизм.
Основные этапы сосудисто-тромбоцитарного гемостаза.
Вы также можете почувствовать легкую боль, когда игла вставляется в вену. В зависимости от человека и в зависимости от количества крови, вы можете почувствовать легкое чувство головокружения. После взятия образца крови у вас могут возникнуть следующие симптомы.
Если вена набухает, нанесите теплый компресс несколько раз в день, если это необходимо. После взятия крови у вас могут быть головокружение или слабость. предотвращает свертывание крови или если вы принимаете антикоагулянты. В противном случае будет очень сложно остановить кровотечение.
- Небольшой взрыв в области, где была вставлена игла.
- После того, как врач потянет иглу, вы должны поддерживать давление на область.
- Это уменьшает риск синяков.
Первый этап - адгезия (прилипание тромбоцитов к месту повреждения, например к субэндотелиальному слою). После этого происходит активация и дегрануляция тромбоцитов (показаны некоторые из веществ, выделяемых тромбоцитами). На последнем этапе происходит агрегация тромбоцитов (связывание активированных тромбоцитов с прилипшими к месту повреждения тромбоцитами).
Также рекомендуется сообщить врачу о любом типе лечения, которое вы принимаете, независимо от того, требуется ли ему рецепт. Если лекарства, которые вы принимаете, рискуют повлиять на результаты теста, ваш врач-специалист закажет прекращение лечения. Процесс коагуляции является одним из самых сложных процессов и возникает в ответ на некоторые сосудистые поражения, которые происходят в организме. Помимо факторов коагуляции, этот процесс также включает участие фибриногена, неферментативных кофакторов и фосфолипидов.
Гемофилия - наследственное генетическое заболевание, которое ставит под угрозу способность к свертыванию крови. Эти факторы действуют в цепочке, в механизме, который предлагает принцип домино. Если один из этих факторов недостаточен, процесс, ведущий к свертыванию, прерывается.
Коагуляционный гемостаз
Свертывание крови – это цепной ферментативный процесс, в котором последовательно происходит активация факторов свертывания и образование их комплексов. Сущность свертывания крови заключается в переходе растворимого белка крови фибриногена в нерастворимый фибрин, в результате чего образуется прочный фибриновый тромб.
Тяжелая форма - 60%, средняя форма - 28%, легкая форма - 2%. . Почему у мальчиков только гемофилия? Гемофилия встречается только у мальчиков; есть очень редкие случаи проявления у девочек. Соответственно, передача гемофилии будет следующей: Мать может быть гемофилией - имеет хроническую Х-хромосому. Шансы на передачу аномалии составляют 50%.
С пораженной Х-хромосомой, взятой у матери, мальчик проявит болезнь. . Шансы на девушке, чтобы показать гемофилии редко: оба родителя должны быть носителями для отправки их детей, пострадавших Х-хромосомы, поэтому компенсация не представляется возможным.
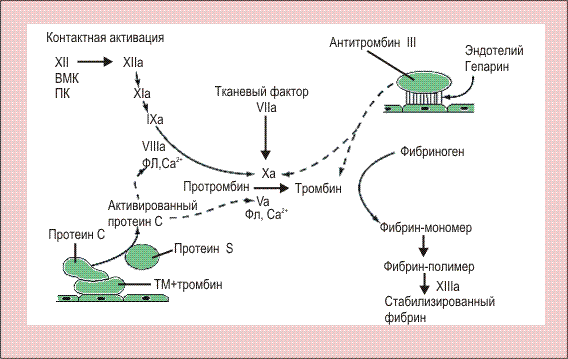
Схема свертывания крови.
Факторы свертывания традиционно обозначаются римскими цифрами, а их активные формы - буквой "а".
Есть два независимых механизма свертывания - внутренний, или контактный, и внешний, зависимый от тканевого фактора. Они сходятся на стадии активации фактора Х и приводят к образованию тромбина, который превращает фибриноген в фибрин. Эти реакции тормозятся антитромбином III, связывающим все факторы свертывания, относящиеся к сериновым протеазам (за исключением фактора VII), а также системой протеин С-протеин S, которая инактивирует факторы V и VIII.
Наиболее распространенное кровотечение не является внешним. Гемофилии, вызванные геморрагиями, обычно возникают в суставах даже при незначительных травмах. Где мы можем иметь воспаление, небольшую гематому, боль более или менее интенсивную, гемофилия будет кровоточить: кровь будет течь и будет накапливаться в суставах. Со время, несчастные случаи и повторные кровотечения влияют кости и суставы теряют свою форму и подвижность, вызывая стойкую нетрудоспособность.
Гемофилия риска кровотечения в других областях тела, внутренние органы, мозг и мышцы. Однако суставное кровотечение наиболее разрушено. Частота возникновения кровотечений.
- Колено - 45%, локоть - 25%, лодыжка - 15%.
- Экстренный, по запросу, дома, профилактический.
ВМК - высокомолекулярный кининоген;
ТМ - тромбомодулин;
ПК - прекалликреин;
ФЛ - фосфолипиды.
Процесс свертывания крови осуществляется в 3 последовательные фазы.
Первая фаза является самой сложной и продолжительной. Во время этой фазы происходит образование активного ферментативного комплекса – протромбиназы, являющейся активатором протромбина. В образовании этого комплекса принимают участие тканевые и кровяные факторы. В результате формируются тканевая и кровяная протромбиназы. Образование тканевой протромбиназы начинается с активации тканевого тромбопластина, образующегося при повреждении стенок сосуда и окружающих тканей. Вместе с VII фактором и ионами кальция он активирует X фактор. В результате взаимодействия активированного X фактора с V фактором и с фосфолипидами тканей или плазмы образуется тканевая протромбиназа. Этот процесс длится 5 – 10 секунд.
Препараты, содержащие факторы коагуляции. Либо продукты крови, либо сконцентрированы с помощью факторов, извлеченных из плазмы, или рекомбинантных факторов. Лечение с помощью продуктов плазмы с высоким риском инфицирования пациента с гепатитом С и другими заболеваниями, которые передаются таким образом. Предпочтительным является лечение концентраций факторов, вызванных плазмой, или рекомбинантных факторов.
Профилактическое лечение обеспечивает нормальную жизнь для гемофилиев. Частота может идти как частота порядка от одного раза в неделю, если меньший дефицит фактора свертывания до трех раз в неделю, в более тяжелых случаях. В случае, если пациент знает, что тело является фактором свертывания крови необходим, чтобы остановить возможное кровотечение, он должен воздержаться от дальнейшей физической активности нормальной для других, но для него опасно. Он знает, что в случае травмы его тело будет реагировать так же, как и здоровый человек.
Образование кровяной протромбиназы начинается с активации XII фактора при его контакте с волокнами коллагена поврежденных сосудов. В активации и действии XII фактора участвуют также высокомолекулярный кининоген (ф XV) и калликреин (ф XIV). Затем XII фактор активирует XI фактор, образуя с ним комплекс. Активный XI фактор совместно с IV фактором активирует IX фактор, который, в свою очередь, активирует VIII фактор, Затем происходит активация X фактора, который образует комплекс с V фактором и ионами кальция, чем и заканчивается образование кровяной протромбиназы. В этом также участвует тромбоцитарный фактор 3. Этот процесс длится 5-10 минут.
Вторая фаза. Образовавшаяся протромбиназа адсорбирует неактивный фермент плазмы протромбин(II фактор) и на своей поверхности превращает его в активный фермент тромбин. В этом процессе принимают участие факторы IV, V, X и факторы тромбоцитов 1и 2. Вторая фаза – образование тромбина – протекает за 2 – 5 с.
Третья фаза. В эту фазу растворимый белок крови фибриноген превращается в нерастворимый фибрин, образующий основу тромба. Вначале под влиянием тромбина происходит образование фибрин-мономера. Затем с участием ионов кальция образуется растворимый фибрин-полимер (фибрин “S”, soluble). Под влиянием фибринстабилизирующего фактора XIII происходит образование нерастворимого фибрин-полимера (фибрин “I”, insoluble), устойчивого к фибринолизу. В фибриновых нитях оседают форменные элементы крови, в частности эритроциты, и формируется кровяной сгусток, или тромб, который закупоривает рану.
После образования сгустка начинается процесс ретракции, т.е. уплотнения и закрепления тромба в поврежденном сосуде. Это происходит с помощью сократительного белка тромбоцитов тромбостенина и ионов кальция. Через 2 – 3 часа сгусток сжимается до 25 – 50% от своего первоначального объема и идет отжатие сыворотки, т.е. плазмы, лишенной фибриногена. За счет ретракции тромб становится более плотным и стягивает края раны.
Фибринолиз
Фибринолиз – это процесс расщепления фибринового сгустка, в результате которого происходит восстановление просвета сосуда. Фибринолиз начинается одновременно с ретракцией сгустка, но идет медленнее. Это тоже ферментативный процесс, который осуществляется под влиянием плазмина (фибринолизина). Плазмин находится в плазме крови в неактивном состоянии в виде плазминогена. Под влиянием кровяных и тканевых активаторов плазминогена происходит его активация. Высокоактивным тканевым активатором является урокиназа. Кровяные активаторы находятся в крови в неактивном состоянии и активируются адреналином, лизокиназами. Плазмин расщепляет фибрин на отдельные полипептидные цепи, в результате чего происходит лизис (растворение) фибринового сгустка,
Если нет условий для фибринолиза, то возможна организация тромба, т.е. замещение его соединительной тканью. Иногда тромб может оторваться от места своего образования и вызвать закупорку сосуда в другом месте (эмболия).
ПЛАЗМЕННЫЕ ФАКТОРЫ СВЕРТЫВАНИЯ КРОВИ
I, или фибриноген
Белок. Образуется в печени. Под влиянием тромбина переходит в фибрин. Участвует в агрегации тромбоцитов. Необходим для репарации тканей
II, или протромбин
Гликопротеид. Образуется в печени в присутствии витамина К. Под влиянием протромбиназы переходит в тромбин (фактор Ив)
Ш, или тромбопластин
Состоит из белка апопротеина III и комплекса фосфолипидов. Входит в состав мембран многих тканей. Является матрицей для развертывания реакций, направленных на образование протромбиназы по внешнему механизму
IV, или ион Са2
Участвует в образовании комплексов, входит в состав протромбиназы. Способствует агрегации тромбоцитов. Связывает гепарин. Принимает участие в ретракции сгустка и тромбоцитарной пробки. Тормозит фибринолиз
V, или акцелератор-глобулин
Белок. Образуется в печени. Активизируется тромбином (фактор Па). Создает оптимальные условия для взаимодействия фактора Ха и протромбина (фактор II)
(VI, исключен из классификации)
VII, или проконвертин
Гликопротеид. Образуется в печени под влиянием витамина К. Принимает участие в формировании протромбиназы по внешнему механизму. Активируется факторами Х11в, Ха, 1Ха, Па и при взаимодействии с тромбопластином (фактор III)
VIII, или антигемофильный глобулин (АГГ). антигемофильный глобулин А
Гликопротеид. Синтезируется в печени, селезенке, лейкоцитах. Образует комплексную молекулу с фактором Виллебранда (FW) и специфическим антигеном. Активируется тромбином. Создает оптимальные условия для взаимодействия факторов 1Ха и X. При его отсутствии возникает заболевание гемофилия А
Компонент комплекса фактора VIII: Образуется эндотелиальными клетками. Обеспечивает устойчивость фактора VIII: С в кровотоке и необходим для адгезии тромбоцитов. При его недостатке развивается болезнь Виллебранда, сопровождающаяся нарушением сосудисто-тромбоцитарного гемостаза
IX, или Кристмас-фактор,
антигемофильный фактор
Гликопротеид. Образуется в печени под влиянием витамина К. Активируется факторами XIa, VIla и IIа. Переводит фактор X в Ха. При его отсутствии возникает заболевание гемофилия В
X, или Стюарт Прауэр-фактор
Гликопротеид. Образуется в печени, под влиянием витамина К. Фактор Ха, являясь протромбиназой, активируется факторами VIla и IХа. Переводит фактор II в IIа
XI, или плазменный предшественник тромбопластина
Гликопротеид. Предполагают, что образуется в печени. Активируется фактором ХIIа калликреином совместно с высокомолекулярным кининогеном (ВМК)
XII, или фактор Хагемана
Белок. Предполагают, что образуется эндотелиальными клетками, лейкоцитами, макрофагами. Активируется отрицательно заряженными поверхностями, адреналином, калликреином. Запускают внешний и внутренний механизм образования протромбиназы и фибринолиза, активирует фактор XI и прекалликреин
ХШ, или фибринстабилизирующий фактор (ФСФ), фибриназа
Глобулин. Синтезируется фибробластами и мегакариоцитами. Стабилизирует фибрин. Необходим для нормального течения репаративных процессов
Фактор Флетчера, или прекалликреин
Белок. Участвует в активации фактора XII, плазминогена и ВМК
Фактор Фитцджеральда, высокомолекулярный кининоген (ВМК)
Является компонентом калликреин-кининовой системы.
Образуется в тканях. Активируется калликреином, принимает участие в активации факторов XII, XI и фибринолиза
Активация плазменных факторов происходит главным образом за счет протеолиза и сопровождается отщеплением пептидных ингибиторов. Активное состояние фактора обозначается присоединением к его номеру буквы «а» (фактор IIа, Va, VIIa и т. д.). Плазменные факторы делят на 2 группы: витамин К-зависимые (образуются преимущественно в печени под влиянием витамина К) и витамин К-независимые (для синтеза которых витамин К не требуется).
В эритроцитах обнаружены многие соединения, аналогичные тромбоцитарным факторам (см. раздел 6.2.3). Важнейшим из них является фосфолипидный фактор, или частичный тромбопластин (напоминает фактор Р3), который входит в состав мембраны. Кроме того, эритроциты содержат большое количество АДФ, фибриназу и другие факторы. При травме сосуда около 1% наименее стойких эритроцитов вытекающей крови разрушается, что способствует образованию тромбоцитарной пробки и фибринового сгустка.
Особенно велика роль эритроцитов в свертывании крови в случае их массового разрушения (переливание несовместимой крови, резус-конфликт матери и плода, гемолитические анемии и др.)
Лейкоциты содержат факторы свертывания, получившие наименование лейкоцитарных. В частности, моноциты и макрофаги при стимуляции антигеном синтезируют белковую часть тромбопластина - апопротеин III, что значительно ускоряет свертывание крови. Эти же клетки являются продуцентами витамин К-зависимых факторов свертывания - II, VII, IX и X. Приведенные факторы являются одной из основных причин возникновения диссеминированного (распространенного) внутрисосудистого свертывания крови (ДВС-синдром) при многих воспалительных и инфекционных заболеваниях, что значительно отягощает течение патологического процесса, а иногда служит причиной смерти больных.
Важная роль в процессе свертывания крови отводится тканевым факторам, к которым в первую очередь относится тромбопластин (фактор 3). Концентрация тромбопластина высока в коре большого мозга, легких, плаценте и стимулированном антигенами эндотелии сосудов. При разрушении тканей и стимуляции эндотелия большое количество тромбопластина поступает в кровоток, что может вызывать развитие ДВС-синдрома.
Механизм свертывания крови
Процесс свертывания крови представляет собой преимущественно проферментно-ферментный каскад, в котором проферменты, переходя в активное состояние, приобретают способность активировать другие факторы свертывания крови. Подобная активация может носить последовательный и ретроградный характер.
Процесс свертывания крови может быть разделен на три фазы: первая включает комплекс последовательных реакций, приводящих к образованию протромбиназы, во вторую фазу осуществляется переход протромбина (фактор II) в тромбин (фактор IIа) и в третью фазу из фибриногена образуется фибрин.
Первая фаза - образование протромбиназы может происходить по внешнему и внутреннему механизму. Внешний механизм предполагает обязательное присутствие тромбопластина (фактор III), внутренний же связан с участием тромбоцитов (фактор Р3) или разрушенных эритроцитов. Вместе с тем внутренний и внешний пути образования протромбиназы имеют много общего, так как активируются одними и теми же факторами (фактор ХIIа, калликреин, ВМК и др.), а также приводят в конечном итоге к появлению одного и того же активного фермента - фактора Ха, выполняющего функции протромбиназы. При этом и полный, и частичный тромбопластин служат матрицами, на которых в присутствии ионов Са2+ развертываются ферментативные реакции.
Формирование протромбиназы по внешнему пути начинается с активации фактора VII при его взаимодействии с тромбопластином и фактором ХIIа. Кроме того, фактор VII может переходить в деятельное состояние под влиянием факторов XIa, IXa, Ха, IIа и калликреина. В свою очередь фактор VIIa не только переводит фактор X в Ха (ведет к появлению протромбиназы), но и активирует фактор IX, участвующий в образовании протромбиназы по внутреннему механизму.
Образование протромбиназы по внешнему пути происходит чрезвычайно быстро (за 20-30 с), ведет к появлению небольших порций тромбина (IIа), который способствует необратимой агрегации тромбоцитов, активации факторов VIII и V и значительно ускоряет формирование протромбиназы по внутреннему механизму. Инициатором внутреннего механизма образования протромбиназы является фактор XII, который активируется травмированной поверхностью стенки сосуда, кожей, коллагеном, адреналином, в лабораторных условиях - при контакте со стеклом, после чего переводит фактор XI в XIa. В этой реакции может принимать участие калликреин (активируется фактором ХIIа) и ВМК (активируется калликреином). Фактор XIa оказывает непосредственное влияние на фактор IX, переводя его в фактор IXa. Специфическая деятельность последнего направлена на протеолиз фактора X и протекает при обязательном участии фактора VIII (или VIIIa).
Следует заметить, что активация фактора X под влиянием комплекса факторов VIII и IXa получила название теназной реакции.
Вторая фаза процесса свертывания крови - переход фактора II в фактор IIа осуществляется под влиянием протромбиназы (фактор Ха) в присутствии фактора V (Va) и сводится к протеолитическому расщеплению протромбина, благодаря чему появляется фермент тромбин, обладающий свертывающей активностью.
Третья стадия процесса свертывания крови - переход фибриногена в фибрин - носит этапный характер. Под влиянием фактора IIа от фибриногена отщепляются фибринопептиды и образуется фибрин-мономер (фактор Im). Из него благодаря процессу полимеризации формируются олигомеры и димеры фибрина (фактор Iо и Id), из которых за счет продольного и поперечного связывания образуются протофибриллы - легкорастворимый фибрин, или фибрин S, быстро лизирующийся под влиянием протеаз (плазмина, трипсина). В дальнейшем в процесс образования фибрина вмешивается фактор XIII (фибриназа, фибринстабилизирующий фактор), который после активации тромбином в присутствии ионов Са2+ «прошивает» фибринполимеры дополнительными перекрестными связями, в результате чего появляется труднорастворимый фибрин, или фибрин i (insoluble). В результате этой реакции сгусток становится резистентным к фибринолитическим (протеолитическим) агентам и плохо поддается разрушению